 Tabla Periódica Ricardo y Miguel Ángel Rojo
Tabla Periódica Ricardo y Miguel Ángel Rojo
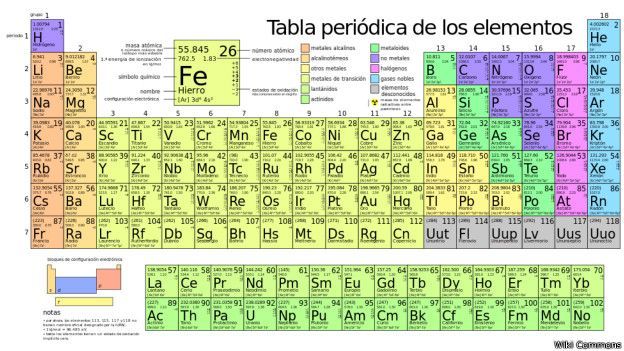
En esta entrada colgaré información buscada en clase de Física y Química acerca de una serie de elementos de la tabla periódica, respondiendo a una serie de preguntas planteadas por el profesor.
Hidrógeno:
- Nombre: Hidrógeno.
- Símbolo: H
- Número atómico: 1
- Masa atómica: 1,00794 u
- Si es sólido, líquido, gas a temperatura ambiente: es gas a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 1
- Grupo: 1
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: constituyentes principales del agua y de toda la materia orgánica. Existen 3 isótopos del hidrógeno: el protio, el deuterio y el tritio, de masa 3. Es extremadamente inflamable.
- Aplicaciones: el empleo más importante del hidrógeno es en la síntesis del amoniaco. Se usa en la refinación del petróleo y en la eliminación del azufre. Se consumen grandes cantidades de hidrógeno en el día a día. Grandes cantidades de hidrógeno se emplean como combustible de cohetes, en combinación con oxígeno o flúor.
Litio:
- Nombre: Litio.
- Símbolo: Li
- Número atómico: 3
- Masa atómica: 6,941 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 2
- Grupo: 1
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal ligero.
- Características más importantes del elemento: el litio es el metal más ligero de todos, incluso tiene una densidad equivalente a casi la mitad que la del agua, pudiendo no sólo flotar en ella sino también reaccionar con ésta y formar gas de hidrógeno e hidróxido de litio. Como ya mencionamos, se trata de un metal alcalino y tiene una apariencia muy particular, teniendo un color plateado (como el Na, el K y la mayoría de los metales alcalinos) que se ve modificado perdiendo lustre al exponerse al aire cuando tiene mucha humedad.
- Aplicaciones: el litio se emplea en aplicaciones de transferencia de calor, y por su elevado potencial electroquímico constituye un ánodo adecuado para las baterías eléctricas... El cloruro de litio y el bromuro de litio tienen una elevada higroscopicidad por lo que son excelentes secantes.
Sodio:
- Nombre: Sodio.
- Símbolo: Na
- Número atómico: 11
- Masa atómica: 22,9898 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 3
- Grupo: 1
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal ligero.
- Características más importantes del elemento: metal blando, ligero y de color plateado que no se encuentra libre en la naturaleza. En las condiciones apropiadas reacciona espontáneamente en el agua. Normalmente no arde en contacto con el aire por debajo de 40 °C.
- Aplicaciones: se usa en la alimentación, en forma de sal. Se usa en la creación de desodorantes, en la creación de placas fotovoltaicas y en la purificación de metales fundidos.
Potasio:
- Nombre: Potasio.
- Símbolo: K
- Número atómico: 19
- Masa atómica: 39,098 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 4
- Grupo: 1
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal ligero.
- Características más importantes del elemento: quinto metal más ligero y liviano; es un sólido blando que se corta con facilidad con un cuchillo, tiene un punto de fusión muy bajo, arde con llama violeta y presenta un color plateado en las superficies expuestas al aire, en cuyo contacto se oxida con rapidez, lo que obliga a almacenarlo recubierto de aceite.
- Aplicaciones: se usa en células fotoeléctricas, en la creación de cristales y transferencia de calor. Además, está presente en los extremos de los cromosomas (en los telómeros) estabilizando la estructura.
Rubidio:
- Nombre: Rubidio.
- Símbolo: Rb
- Número atómico: 37
- Masa atómica: 85,47 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 5
- Grupo: 1
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal ligero.
- Características más importantes del elemento: el rubidio es un tipo de metal blando y alcalino que presenta un característico color blanco platinado. A temperatura ambiente, el rubidio se vuelve líquido con facilidad y es un elemento altamente reactivo; de hecho, el rubidio es el segundo elemento más electropositivo entre los del grupo de los alcalinos.
- Aplicaciones: se utiliza principalmente en la fabricación de cristales especiales para sistemas de telecomunicaciones de fibra óptica y equipos de visión nocturna. Otros usos son: Recubrimientos fotoemisores de telurio-rubidio en células fotoeléctricas y detectores electrónicos.
Cesio:
- Nombre: Cesio.
- Símbolo: Cs
- Número atómico: 55
- Masa atómica: 132,905 u
- Si es sólido, líquido, gas a temperatura ambiente: es líquido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 6
- Grupo: 1
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal ligero.
- Características más importantes del elemento: metal blando, ligero y de bajo punto de fusión. Es el segundo menos electronegativo de todos los elementos después del francio. El cesio reacciona en forma vigorosa con oxígeno para formar una mezcla de óxidos. En aire húmedo, el calor de oxidación puede ser suficiente para fundir y prender el metal.
- Aplicaciones: en celdas fotoeléctricas, instrumentos espectrográficos, contadores de centelleo, bulbos de radio, lámparas militares de señales infrarrojas y varios aparatos ópticos y de detección.
Francio:
- Nombre: Francio.
- Símbolo: Fr
- Número atómico: 87
- Masa atómica: 223 u
- Si es sólido, líquido, gas a temperatura ambiente: es líquido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 7
- Grupo: 1
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal ligero.
- Características más importantes del elemento: su electronegatividad es la más baja conocida y es el segundo elemento menos abundante en la naturaleza (el primero es el astato). El francio es un metal alcalino altamente radiactivo y reactivo que se desintegra generando astato, radio y radón.
- Aplicaciones: no hay aplicaciones comerciales para el francio debido a su escasez y a su inestabilidad. Sólo ha sido usado en tareas de investigación, tanto en el campo de la biología como en el de la estructura atómica.
Berilio:
- Nombre: Berilio.
- Símbolo: Be
- Número atómico: 4
- Masa atómica: 9,012182 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 2
- Grupo: 2
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal ligero.
- Características más importantes del elemento: es un material tóxico, de color gris, duro, ligero y quebradizo.
- Aplicaciones: en el diagnóstico con rayos X se usan delgadas láminas de berilio para filtrar la radiación visible, así como en la litografía de rayos X para la reproducción de circuitos integrados. Se usa también como moderador de neutrones en reactores nucleares. Por su rigidez, ligereza y estabilidad dimensional, se emplea en la construcción de diversos dispositivos como giroscopios, equipo informático, muelles de relojería e instrumental diverso.
Magnesio:
- Nombre: Magnesio.
- Símbolo: Mg
- Número atómico: 12
- Masa atómica: 24,305 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 3
- Grupo: 2
- Metal ligero, metal de transición, metal, no metal o gas noble: metal ligero.
- Características más importantes del elemento: séptimo elemento en abundancia constituyendo del orden del 2 % de la corteza terrestre y el tercero más abundante disuelto en el agua de mar. El ion magnesio es esencial para todas las células vivas. El metal puro no se encuentra en la naturaleza.
- Aplicaciones: se usa como material refractario en hornos para la producción de hierro y acero, metales no férreos, cristal y cemento, así como en agricultura e industrias químicas y de construcción.
Calcio:
- Nombre: Calcio.
- Símbolo: Ca
- Número atómico: 20
- Masa atómica: 40,078 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 4
- Grupo: 2
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal ligero.
- Características más importantes del elemento: es un metal blando, grisáceo, y es el quinto más abundante en masa de la corteza terrestre. También es el ion más abundante disuelto en el agua de mar, tanto como por su molaridad y como por su masa, después del sodio, cloruros, magnesio y sulfatos.
- Aplicaciones: es un agente reductor en la extracción de otros metales como el uranio, circonio y torio, también es un desoxidante, desulfurizador, o decarburizador para varias aleaciones ferrosas y no ferrosas, es un agente de aleación utilizado en la producción de aluminio, berilio, cobre, plomo y magnesio y tiene aplicaciones en muchos productos lácteos o medicamentos para el refuerzo de los huesos. La falta de calcio en los huesos humanos facilita la aparición de enfermedades como la osteoporosis.
Estroncio:
- Nombre: Estroncio.
- Símbolo: Sr
- Número atómico: 38
- Masa atómica: 87,62 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 5
- Grupo: 2
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal ligero.
- Características más importantes del elemento: es un metal blando de color plateado brillante, algo maleable, también alcalino térreo, que rápidamente se oxida en presencia de aire adquiriendo un tono amarillento por la formación de óxido, por lo que debe conservarse sumergido en parafina. Debido a su elevada creatividad el metal se encuentra en la naturaleza combinado con otros elementos formando compuestos.
- Aplicaciones: el uso más destacado del estroncio dentro de la ciencia es el de la construcción de los relojes atómicos más modernos y precisos que se conocen, superando por varios "ceros" al los relojes atómicos de Cesio hasta ahora usados.
Bario:
- Nombre: Bario.
- Símbolo: Ba
- Número atómico: 56
- Masa atómica: 137,33 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 6
- Grupo: 2
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal ligero.
- Características más importantes del elemento: es un elemento metálico que es químicamente similar al calcio, pero más reactivo. Este metal se oxida con mucha facilidad cuando se expone al aire y es altamente reactivo con el agua o el alcohol, que produce gas hidrógeno. Se quema con el aire o el oxígeno, no sólo produce el óxido de bario (BaO), sino también el peróxido. Los compuestos de este elemento pesado se destacan por su alto peso específico.
- Aplicaciones: el bario se usa en pirotecnia, como muchos otros elementos de los grupos A. El bario metálico tiene pocas aplicaciones prácticas, aunque a veces se usa para recubrir conductores eléctricos en aparatos electrónicos y en sistemas de encendido de automóviles. El nitrato de bario se utiliza en fuegos artificiales, y el carbonato de bario en venenos para ratas (por medio de la ingesta).
Radio:
- Nombre: Radio.
- Símbolo: Ra
- Número atómico: 88
- Masa atómica: 226 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 7
- Grupo: 2
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal ligero.
- Características más importantes del elemento: es el más pesado de los metales alcalinotérreos, es intensamente radiactivo y se parece químicamente al bario. Los preparados de radio son destacables porque son capaces de mantenerse a más alta temperatura que su entorno y por sus radiaciones, que pueden ser de tres tipos: rayos alfa, rayos beta y rayos gamma. Además, el radio produce neutrones si se mezcla con berilio.
- Aplicaciones: cuando se mezcla con berilio, es una fuente de neutrones para experimentos físicos. El cloruro de radio se usa en medicina para producir radón, que se usa en tratamientos contra el cáncer. Una unidad de radiactividad, el curio, está basada en la radiactividad del radio-226.
Boro:
- Nombre: Boro.
- Símbolo: B
- Número atómico: 5
- Masa atómica: 10,81 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 2
- Grupo: 13
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: es un elemento metaloide, semiconductor, trivalente que existe abundantemente en el mineral bórax. Hay dos alótropos del boro; el boro amorfo es un polvo marrón, pero el boro metálico es negro.
- Aplicaciones: el compuesto de boro de mayor importancia económica es el bórax que se emplea en grandes cantidades en la fabricación de fibra de vidrio aislante y perborato de sodio.
Aluminio:
- Nombre: Aluminio.
- Símbolo: Al
- Número atómico: 13
- Masa atómica: 26,982 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 3
- Grupo: 13
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: es un elemento muy abundante en la naturaleza, solo aventajado por el oxígeno y el silicio. Se trata de un metal ligero, con una densidad de 2700 kg/m³, y con un bajo punto de fusión (660 °C). Su color es grisáceo y refleja bien la radiación electromagnética del espectro visible y el térmico.
- Aplicaciones: se usa en forma pura, aleado con otros metales o en compuestos no metálicos. En estado puro se aprovechan sus propiedades ópticas para fabricar espejos domésticos e industriales, como pueden ser los de los telescopios reflectores. Su uso más popular, sin embargo, es como papel aluminio, que consiste en láminas de material con un espesor tan pequeño que resulta fácilmente maleable y apto por tanto para embalaje alimentario. También se usa en la fabricación de latas y tetrabriks.
Galio:
- Nombre: Galio.
- Símbolo: Ga
- Número atómico: 31
- Masa atómica: 69,723 u
- Si es sólido, líquido, gas a temperatura ambiente: es líquido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 4
- Grupo: 13
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: es un metal blando, grisáceo en estado líquido y plateado brillante al solidificar, sólido deleznable a bajas temperaturas que funde a temperaturas cercanas a la del ambiente como, el cesio, mercurio y rubidio e incluso cuando se sostiene en la mano por su bajo punto de fusión (28,56 °C).
- Aplicaciones: se usa en la fabricación de componentes electrónicos como transistores, rectificadores, células fotoeléctricas y diodos láser y máser. También se usa en algunos tipos de aleaciones, como el metal Wiga (Sn, Bi y Ga).
Indio:
- Nombre: Indio.
- Símbolo: In
- Número atómico: 49
- Masa atómica: 114,82 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 5
- Grupo: 13
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: es un metal blanco plateado, muy blando, que presenta un lustre brillante. Cuando se dobla el metal emite un sonido característico. Su estado de oxidación más característico es el +3, aunque también presenta el +2 en algunos compuestos.
- Aplicaciones: se empleó principalmente durante la Segunda Guerra Mundial como recubrimiento en motores aeronáuticos de alto rendimiento. Después de esto se ha destinado a nuevas aplicaciones en aleaciones, en soldadura y en la industria electrónica.
Talio:
- Nombre: Talio.
- Símbolo: Tl
- Número atómico: 81
- Masa atómica: 204,38 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 6
- Grupo: 13
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: es muy blando y maleable; se puede cortar con un cuchillo. Al ser expuesto al aire pasa de presentar un brillo metálico a rápidamente empañarse con un tono gris azulado parecido al plomo.
- Aplicaciones: es inodoro e insípido fue usado para exterminar ratas y hormigas. Desde 1972 su uso fue prohibido en Estados Unidos a causa de su toxicidad. Otros países siguieron el ejemplo en los años siguientes. Las sales de talio se usaron como tratamiento de dermatofitosis, otras infecciones de la piel y para reducir la sudoración nocturna de los pacientes con tuberculosis.
Nihonium (Nihonio):
- Nombre: Nihonium (Nihonio).
- Símbolo: Nh
- Número atómico: 113
- Masa atómica: 286 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es sintético.
- Periodo: 7
- Grupo: 13
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: es un elemento muy inestable.
- Aplicaciones: por su vida media tan reducida de tan solo milisegundos a minutos y su inestabilidad son nulas las aplicaciones industriales o comerciales de este elemento súper pesado, por lo que su aplicación se relega solo a la investigación científica.
Carbono:
- Nombre: Carbono.
- Símbolo: C
- Número atómico: 6
- Masa atómica: 12,011 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 2
- Grupo: 14
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: es un elemento notable por varias razones. Sus formas alotrópicas incluyen, una de las sustancias más blandas (el grafito) y una de las más duras (el diamante) y, desde el punto de vista económico, es de los materiales más baratos (carbón) y uno de los más caros (diamante). Más aún, presenta una gran afinidad para enlazarse químicamente con otros átomos pequeños, incluyendo otros átomos de carbono con los que puede formar largas cadenas, y su pequeño radio atómico le permite formar enlaces múltiples.
- Aplicaciones: el principal uso industrial del carbono es como un componente de hidrocarburos, especialmente los combustibles fósiles (petróleo y gas natural). Del primero se obtienen, por destilación en las refinerías, gasolinas, keroseno y aceites, siendo además la materia prima empleada en la obtención de plásticos. El segundo se está imponiendo como fuente de energía por su combustión más limpia.
Silicio:
- Nombre: Silicio.
- Símbolo: Si
- Número atómico: 14
- Masa atómica: 28,085 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 3
- Grupo: 14
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: sus propiedades son intermedias entre las del carbono y el germanio. En forma cristalina es muy duro y poco soluble y presenta un brillo metálico y color grisáceo. Aunque es un elemento relativamente inerte y resiste la acción de la mayoría de los ácidos, reacciona con los halógenos y álcalis diluidos. El silicio transmite más del 95 % de las longitudes de onda de la radiación infrarroja.
- Aplicaciones: se utiliza en aleaciones, en la preparación de las siliconas, en la industria de la cerámica técnica y, debido a que es un material semiconductor muy abundante, tiene un interés especial en la industria electrónica y microelectrónica como material básico para la creación de obleas o chips que se pueden implantar en transistores, pilas solares y una gran variedad de circuitos electrónicos.
Germanio:
- Nombre: Germanio.
- Símbolo: Ge
- Número atómico: 32
- Masa atómica: 72,630 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 4
- Grupo: 14
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: es un semimetal, de color blanco grisáceo lustroso, quebradizo, que conserva el brillo a temperaturas ordinarias. Presenta la misma estructura cristalina que el diamante y resiste a los ácidos y álcalis.
- Aplicaciones: las aplicaciones del germanio se ven limitadas por su elevado costo y en muchos casos se investiga su sustitución por materiales más económicos.
Estaño:
- Nombre: Estaño.
- Símbolo: Sn
- Número atómico: 50
- Masa atómica: 118,71 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 5
- Grupo: 14
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: es un metal plateado, maleable, que se oxida fácilmente, a temperatura ambiente, cambiando de color a un gris más opaco, y es resistente a la corrosión. Se encuentra en muchas aleaciones y se usa para recubrir otros metales protegiéndolos de la corrosión.
- Aplicaciones: se usa como protector del oro, del acero y de diversos metales usados en la fabricación de latas de conserva. También se usa para disminuir la fragilidad del vidrio. Los compuestos de estaño se usan para fungicidas, tintes, dentífricos y pigmentos. Se usa para realizar bronce, aleación de estaño y cobre.
Plomo:
- Nombre: Plomo.
- Símbolo: Pb
- Número atómico: 82
- Masa atómica: 207,2 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 6
- Grupo: 14
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: los compuestos de plomo más utilizados en la industria son los óxidos de plomo, el tetraetilo de plomo y los silicatos de plomo. El plomo forma aleaciones con muchos metales, y, en general, se emplea en esta forma en la mayor parte de sus aplicaciones. Es un metal pesado y tóxico, y la intoxicación por plomo se denomina como saturnismo o plumbosis.
- Aplicaciones: su utilización como cubierta para cables, ya sea la de teléfono, de televisión, de internet o de electricidad, sigue siendo una forma de empleo adecuada. La ductilidad única del plomo lo hace muy apropiado para esta aplicación, porque puede estirarse para formar un forro continuo alrededor de los conductos internos.
Flerovio:
- Nombre: Flerovio.
- Símbolo: Fl
- Número atómico: 114
- Masa atómica: 287 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es sintético.
- Periodo: 7
- Grupo: 14
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: se han observado alrededor de 80 desintegraciones de átomos de flerovio, 50 de ellas directamente y 30 de la desintegración de los elementos más pesados Livermorio y Ununoctio.
- Aplicaciones: al ser un elemento tan poco conocido y tan escaso (apenas unos pocos átomos se han creado desde su descubrimiento), este elemento es de lo más inútil.
Nitrógeno:
- Nombre: Nitrógeno.
- Símbolo: N
- Número atómico: 7
- Masa atómica: 14,007 u
- Si es sólido, líquido, gas a temperatura ambiente: es gas a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 2
- Grupo: 15
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: constituye del orden del 78 % del aire atmosférico. En ocasiones es llamado ázoe —antiguamente se usó también Az como símbolo del nitrógeno.
- Aplicaciones: la aplicación comercial más importante del nitrógeno diatómico es la obtención de amoníaco por el proceso de Haber. El amoníaco se emplea con posterioridad en la fabricación de fertilizantes y ácido nítrico.
Fósforo:
- Nombre: Fósforo.
- Símbolo: P
- Número atómico: 15
- Masa atómica: 30,974 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 3
- Grupo: 15
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: el fósforo es un componente esencial de los organismos. Forma parte de los ácidos nucleicos (ADN y ARN). Forma parte de los huesos y dientes de los animales.
- Aplicaciones: los compuestos comerciales más importantes de fósforo son el ácido fosfórico y sus sales, llamadas fosfatos. La mayoría de los compuestos fosforados se usan como fertilizantes. Los compuestos fosforados se usan también para aclarar las soluciones de azúcar de remolacha y en aleaciones especiales como bronces al fósforo. El fósforo blanco se usa en la elaboración de veneno para las ratas, insecticidas y en la industria pirotécnica y el fósforo rojo se usa para fabricar cerillas.
Arsénico:
- Nombre: Arsénico.
- Símbolo: As
- Número atómico: 33
- Masa atómica: 74,92 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 4
- Grupo: 15
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: a presión atmosférica el arsénico sublima a 613 °C, y a 400 °C arde con llama blanca formando el sesquióxido As4O6. Reacciona violentamente con el cloro y se combina, al calentarse, con la mayoría de los metales para formar el arseniuro correspondiente y con el azufre. No reacciona con el ácido clorhídrico en ausencia de oxígeno, pero sí con el nítrico caliente, sea diluido o concentrado y otros oxidantes como el peróxido de hidrógeno, ácido perclórico, etc. Es insoluble en agua pero muchos de sus compuestos lo son.
- Aplicaciones: se usa como preservante de la madera (arseniato de plomo y cromo), uso que representa, según algunas estimaciones, cerca del 70 % del consumo mundial de arsénico. El arseniuro de galio es un importante material semiconductor empleado en circuitos integrados más rápidos, y caros, que los de silicio. También se usa en la construcción de diodos láser y LED. Aditivo en aleaciones de plomo y latones.
Antimonio:
- Nombre: Antimonio.
- Símbolo: Sb
- Número atómico: 51
- Masa atómica: 121,76 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 5
- Grupo: 15
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: el antimonio en su forma elemental es un sólido cristalino, fundible, quebradizo, blanco plateado que presenta una conductividad eléctrica y térmica baja y se evapora a bajas temperaturas. Este elemento semimetálico se parece a los metales en su aspecto y propiedades físicas, pero se comportan químicamente como un no metal. También puede ser atacado por ácidos oxidantes y halógenos.
- Aplicaciones: el antimonio tiene una creciente importancia en la industria de semiconductores en la producción de diodos, detectores infrarrojos.
Bismuto:
- Nombre: Bismuto.
- Símbolo: Bi
- Número atómico: 83
- Masa atómica: 208,98 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 6
- Grupo: 15
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: el bismuto flota sobre su estado líquido, por tener menor densidad en el estado sólido. Esta característica es compartida con el agua, el galio, el ácido acético, el antimonio y el silicio.
- Aplicaciones: la diferencia entre las densidades del plomo (densidad 11.32 g·cm−3) y del bismuto (densidad 9.78 g·cm−3) es lo suficientemente pequeña para que pueda ser utilizado en lugar del plomo en numerosos usos en balística y como balasto. Por ejemplo, puede reemplazar al plomo como material en plomadas para la pesca. Al ser el bismuto un elemento denso con un peso atómico elevado, es utilizado para fabricar escudos de látex impregnados con bismuto para protección de los rayos-X durante exámenes médicos, tales como tomografías computarizadas con rayos X, principalmente porque se le considera un elemento no tóxico.
Moscovium (Moscovio):
- Nombre: Moscovium (Moscovio).
- Símbolo: Mc
- Número atómico: 115
- Masa atómica: 288 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es sintético.
- Periodo: 7
- Grupo: 15
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: es un elemento muy inestable.
- Aplicaciones: usos actualmente desconocidos. Se limitan solamente a la investigación.
Oxigeno:
- Nombre: Oxígeno.
- Símbolo: O
- Número atómico: 8
- Masa atómica: 15,999 u
- Si es sólido, líquido, gas a temperatura ambiente: es gas a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 2
- Grupo: 16
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: en condiciones normales de presión y temperatura, el oxígeno es un gas incoloro e inodoro con fórmula molecular O2, en el que dos átomos de oxígeno se enlazan con una configuración electrónica en estado triplete. Este enlace tiene un orden de enlace de dos y se suele simplificar en las descripciones como un enlace doble o como una combinación de un enlace de dos electrones y dos enlaces de tres electrones.
- Aplicaciones: el 55 % de la producción mundial de oxígeno se consume en la producción de acero Otro 25 % se dedica a la industria química. Del 20 % restante la mayor parte se usa para aplicaciones medicinales, oxicorte, como oxidante en combustible de cohetes y en tratamiento de aguas.
Azufre:
- Nombre: Azufre.
- Símbolo: S
- Número atómico: 16
- Masa atómica: 32,07 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 3
- Grupo: 16
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: este no metal tiene un color amarillento fuerte, amarronado o anaranjado y arde con llama de color azul, desprendiendo dióxido de azufre. Es insoluble en agua pero se disuelve en disulfuro de carbono y benceno.
- Aplicaciones: el azufre se usa en multitud de procesos industriales, como la producción de ácido sulfúrico para baterías, la fabricación de pólvora y el vulcanizado del caucho. Los sulfitos se usan para blanquear el papel y en fósforos. El tiosulfato de sodio o amonio se emplea en la industria fotográfica como «fijador» ya que disuelve el bromuro de plata; y el sulfato de magnesio (sal de Epsom) tiene usos diversos como laxante, exfoliante, o suplemento nutritivo para plantas.
Selenio:
- Nombre: Selenio.
- Símbolo: Se
- Número atómico: 34
- Masa atómica: 78,971 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 4
- Grupo: 16
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: el selenio se puede encontrar en varias formas alotrópicas. El selenio amorfo existe en tres formas, la vítrea, negra, obtenida al enfriar rápidamente el selenio líquido, funde a 180 °C y tiene una densidad de 4,28 g/cm3; la roja, coloidal, se obtiene en reacciones de reducción; el selenio gris cristalino de estructura hexagonal, la forma más común, funde a 220,5 °C y tiene una densidad de 4,81 g/cm3; y la forma roja, de estructura monoclínica, funde a 221 °C y tiene una densidad de 4,39 g/cm3.
- Aplicaciones: se usa con diversos fines. Su derivado, el selenio de amonio, por ejemplo, se ocupa en la fabricación de vidrio. Otro derivado, el sulfuro de selenio, se usa en lociones y champúes como tratamiento para la dermatitis seborreica.
Teluro:
- Nombre: Teluro.
- Símbolo: Te
- Número atómico: 52
- Masa atómica: 127,5 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 5
- Grupo: 16
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: el telurio o teluro es un elemento químico cuyo símbolo es Te y su número atómico es 52. Es un metaloide que se encuentra en el grupo 16 y el periodo 5 de la Tabla periódica de los elementos.
- Aplicaciones: las aplicaciones comunes del teluro: Fotovoltaica, electrónica y semiconductores: Los paneles fotovoltaicos de CdTe de capa delgada son el segmento con mayor crecimiento de la industria solar. El telururo de bismuto (Bi2Te3) se utiliza en dispositivos de refrigeración termoeléctricos (TEC).
Polonio:
- Nombre: Polonio.
- Símbolo: Po
- Número atómico: 84
- Masa atómica: 209 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 6
- Grupo: 16
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: esta sustancia se disuelve con mucha facilidad en ácidos, pero es sólo ligeramente soluble en alcalinos. Está químicamente relacionado con el teluro y el bismuto. El polonio es un metal volátil, reducible al 50% tras 45 horas al aire a una temperatura de 54,8 °C (328 K). Ninguno de los alrededor de 50 isótopos de polonio es estable. Es extremadamente tóxico y altamente radiactivo. Se ha encontrado polonio en minerales de uranio, humo de tabaco y como contaminante. Todos los elementos a partir del polonio son significativamente radiactivos. Se encuentra en el grupo 16 y su número atómico es 84.
- Aplicaciones: Mezclado o aleado con berilio, el polonio puede ser una fuente de neutrones. Se utiliza también en dispositivos destinados a la eliminación de carga estática, en cepillos especiales para eliminar el polvo acumulado en películas fotográficas y también en fuentes de calor para satélites artificiales o sondas espaciales.
Livermorio:
- Nombre: Livermorio.
- Símbolo: Lv
- Número atómico: 116
- Masa atómica: 291 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es sintético.
- Periodo: 7
- Grupo: 16
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: Características generales y propiedades del livermorio. Este elemento transactínido, poco conocido y similar a los que venimos viendo últimamente, recibió su nombre por el Laboratorio Nacional Lawrence Livermore de California, en donde su descubrimiento fue anunciado oficialmente en diciembre del 2000.
- Aplicaciones: usos actualmente desconocidos. Se limitan solamente a la investigación.
Flúor:
- Nombre: Flúor.
- Símbolo: F
- Número atómico: 9
- Masa atómica: 18,998 u
- Si es sólido, líquido, gas a temperatura ambiente: es gas a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 1
- Grupo: 17
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: el flúor es el elemento más electronegativo y reactivo y forma compuestos con prácticamente todo el resto de elementos, incluyendo los gases nobles xenón y radón. Su símbolo es F. Incluso en ausencia de luz y a bajas temperaturas, el flúor reacciona explosivamente con el hidrógeno.
- Aplicaciones: el politetrafluoroetileno (PTFE), también denominado teflón, se obtiene a través de la polimerización de tetrafluoroetileno que a su vez es generado a partir de clorodifluorometano, que se obtiene finalmente a partir de la fluoración del correspondiente derivado halogenado con fluoruro de hidrógeno (HF). También a partir de HF se obtienen clorofluorocarburos (CFC), hidroclorofluorocarburos (HClFC) e hidrofluorocarburos (HFC). Se emplea flúor en la síntesis del hexafluoruro de uranio, UF6, es el gas más pesado conocido y se emplea en el enriquecimiento de uranio 235U.
Cloro:
- Nombre: Cloro.
- Símbolo: Cl
- Número atómico: 17
- Masa atómica: 35,45 u
- Si es sólido, líquido, gas a temperatura ambiente: es gas a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 3
- Grupo: 17
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: en la naturaleza no se encuentra en estado puro ya que reacciona con rapidez con muchos elementos y compuestos químicos, por esta razón se encuentra formando parte de cloruros (especialmente en forma de cloruro de sodio), cloritos y cloratos , en las minas de sal y disuelto en el agua de mar.
- Aplicaciones: las principales aplicaciones de cloro son en la producción de un amplio rango de productos industriales y para consumo. Por ejemplo, es utilizado en la elaboración de plásticos, solventes para lavado en seco y desgrasado de metales, producción de agroquímicos y fármacos, insecticidas, colorantes y tintes, etc.
Bromo:
- Nombre: Bromo.
- Símbolo: Br
- Número atómico: 35
- Masa atómica: 79,904 u
- Si es sólido, líquido, gas a temperatura ambiente: es líquido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 4
- Grupo: 17
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: es corrosivo, resulta peligroso para la salud y debe manipularse con sumo cuidado. A temperatura ambiente, el bromo se evapora con gran facilidad y ese vapor se caracteriza por un intenso olor fétido y de color rojo que resulta muy irritante para la garganta y los ojos.
- Aplicaciones: las aplicaciones químicas e industriales del bromo son numerosas y variadas, destacando los compuestos organobromados, los cuales son preparados a partir de bromo diatómico o bien de bromuro de hidrógeno (ácido bromhídrico en disolución acuosa). La prueba del bromo consiste en el uso de agua de bromo con el objetivo de detectar la presencia de compuestos orgánicos insaturados.
Yodo:
- Nombre: Yodo.
- Símbolo: I
- Número atómico: 53
- Masa atómica: 126,90 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 5
- Grupo: 17
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: al igual que todos los halógenos, forma un gran número de moléculas con otros elementos, pero es el menos reactivo de los elementos del grupo, y tiene ciertas características metálicas. Puede presentar diversos estados de oxidación: −1, +1, +3, +5, +7. Reacciona con el mercurio y el azufre.
- Aplicaciones: se utiliza ampliamente en la industria farmacéutica, como materia prima para los medios de contraste en exámenes de rayos X y en antisépticos, así como catalizador o reactivo en la síntesis de numerosos ingredientes farmacéuticos activos tales como antibióticos, corticoides y fármacos cardiovasculares.
Astato:
- Nombre: Astato.
- Símbolo: At
- Número atómico: 85
- Masa atómica: 210 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 6
- Grupo: 17
- Metal ligero, metal de transición, metal, no metal o gas noble: es un no metal.
- Características más importantes del elemento: el comportamiento químico de este elemento altamente radiactivo es muy similar al de otros halógenos, especialmente el yodo. Se piensa que el ástato es más metálico que el yodo. Investigadores del Laboratorio Nacional de Brookhaven han realizado experimentos en los que se han identificado y medido reacciones elementales que involucran al ástato.
- Aplicaciones: el astato es el elemento químico más raro de la Tierra. En la tabla periódica se representa con el símbolo At y el número atómico 85. ... En la naturaleza, este elemento químico es rarísimo. De hecho, la cantidad total de astato sobre la corteza terrestre no supera lo 28 gramos.
Tenessine (Tenessino):
- Nombre: Tenessine (Tenessino).
- Símbolo: Ts
- Número atómico: 117
- Masa atómica: 294 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es sintético.
- Periodo: 7
- Grupo: 17
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal.
- Características más importantes del elemento: es un elemento muy inestable.
- Aplicaciones: usos actualmente desconocidos. Se limitan solamente a la investigación.
Helio:
- Nombre: Helio.
- Símbolo: He
- Número atómico: 2
- Masa atómica: 4,00 u
- Si es sólido, líquido, gas a temperatura ambiente: es gas a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 1
- Grupo: 18
- Características más importantes del elemento: a pesar de que la configuración electrónica del helio es 1s², no figura en el grupo 2 de la tabla periódica de los elementos, junto al hidrógeno en el bloques, sino que se coloca en el grupo 18 del bloque p, ya que al tener el nivel de energía completo presenta las propiedades de un gas noble.
- Aplicaciones: el helio es más ligero que el aire y a diferencia del hidrógeno no es inflamable, siendo además su poder ascensional un 8 % menor que el de este, por lo que se emplea como gas de relleno en globos y zepelines publicitarios, de investigación atmosférica e incluso para realizar reconocimientos militares.
Neón:
- Nombre: Neón.
- Símbolo: Ne
- Número atómico: 10
- Masa atómica: 20,180 u
- Si es sólido, líquido, gas a temperatura ambiente: es gas a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 2
- Grupo: 18
- Metal ligero, metal de transición, metal, no metal o gas noble: es un gas noble.
- Características más importantes del elemento: es el segundo gas noble más ligero, y presenta un poder de refrigeración, por unidad de volumen, 40 veces mayor que el del helio líquido y tres veces mayor que el del hidrógeno líquido. En la mayoría de las aplicaciones el uso de neón líquido es más costoso que el del helio, ya que es mucho más raro y difícil de conseguir.
- Aplicaciones: el tono rojo-anaranjado de la luz emitida por los tubos de neón se usa abundantemente para los indicadores publicitarios, también reciben la denominación de tubos de neón otros de color distinto que en realidad contienen gases diferentes. Otros usos del neón que pueden citarse son: rotulo luminoso que funciona con neon, indicadores de alto voltaje, tubos de televisión, junto con el helio se emplea para obtener un tipo de láser, el neón licuado se comercializa como refrigerante criogénico y el neón líquido se utiliza en lugar del hidrógeno líquido para refrigeración.
Argón:
- Nombre: Argón.
- Símbolo: Ar
- Número atómico: 18
- Masa atómica: 39,95 u
- Si es sólido, líquido, gas a temperatura ambiente: es gas a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 3
- Grupo: 18
- Metal ligero, metal de transición, metal, no metal o gas noble: es un gas noble.
- Características más importantes del elemento: el argón es soluble en agua y es incoloro e inodoro tanto en estado gaseoso como en estado líquido. En ningún estado de la materia es tóxico. Se le considera un gas muy inerte y aún no se conocen compuestos químicos verdaderos que puedan formarse con él.
- Aplicaciones: se emplea como gas de relleno en lámparas incandescentes ya que no reacciona con el material del filamento incluso a alta temperatura y presión, prolongando de este modo la vida útil de la bombilla, y en sustitución del neón en lámparas fluorescentes cuando se desea un color verde-azul en vez del rojo del neón.
Criptón:
- Nombre: Criptón.
- Símbolo: Kr
- Número atómico: 36
- Masa atómica: 83,798 u
- Si es sólido, líquido, gas a temperatura ambiente: es gas a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 4
- Grupo: 18
- Metal ligero, metal de transición, metal, no metal o gas noble: es un gas noble.
- Características más importantes del elemento: es un gas noble inodoro e insípido de poca reactividad caracterizado por un espectro de líneas verde y rojo-naranja muy brillantes. Es uno de los productos de la fisión nuclear del uranio. El kriptón sólido es blanco, de estructura cristalina cúbica centrada en las caras al igual que el resto de gases nobles.
- Aplicaciones: la mayoría de sus usos están relacionados con la iluminación, se usa en los flash para tomar fotografías, como combustible experimental y como fuente de luz en equipos médicos.
Xenón:
- Nombre: Xenón.
- Símbolo: Xe
- Número atómico: 54
- Masa atómica: 131,29 u
- Si es sólido, líquido, gas a temperatura ambiente: es gas a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 5
- Grupo: 18
- Metal ligero, metal de transición, metal, no metal o gas noble: es un gas noble.
- Características más importantes del elemento: El xenón es un miembro de los elementos de valencia ocho llamados gases nobles o inertes. La palabra "inerte" ya no se usa para describir esta serie química, dado que algunos elementos de valencia cero forman compuestos. En un tubo lleno de gas xenón, se emite un brillo azul cuando se le excita con una descarga eléctrica.
- Aplicaciones: El uso principal y más famoso de este gas es en la fabricación de dispositivos emisores de luz tales como lámparas bactericidas, tubos electrónicos, lámparas estroboscópicas y flashes fotográficos, así como en lámparas usadas para excitar láseres de rubí, que generan de esta forma luz coherente.
Radón:
- Nombre: Radón.
- Símbolo: Rn
- Número atómico: 86
- Masa atómica: 222 u
- Si es sólido, líquido, gas a temperatura ambiente: es gas a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 6
- Grupo: 18
- Metal ligero, metal de transición, metal, no metal o gas noble: es un gas noble.
- Características más importantes del elemento: es un elemento químico perteneciente al grupo de los gases nobles. En su forma gaseosa es incoloro, inodoro e insípido y en forma sólida su color es rojizo. En la tabla periódica tiene el número 86 y símbolo Rn.
- Aplicaciones: este gas noble al congelarse se vuelve fosforescente, los colores van del naranja rojizo al amarillo, y cuando se condensa toma una coloración rojiza intensa. Posee tres isótopos naturales más 22 isótopos que no han sido sintetizados a través de reacciones nucleares, las cuales se llevan a cabo en ciclotrones y aceleradores lineales, siendo el isótopo R-226 el que tiene un promedio de vida más largo.
Oganesson (Oganesón):
- Nombre: Oganesson (Oganesón).
- Símbolo: Og
- Número atómico: 118
- Masa atómica: 294 u
- Si es sólido, líquido, gas a temperatura ambiente: es gas a temperatura ambiente.
- Si es natural o sintético: es sintético.
- Periodo: 7
- Grupo: 18
- Metal ligero, metal de transición, metal, no metal o gas noble: es un gas noble.
- Características más importantes del elemento: es un elemento muy inestable.
- Aplicaciones: usos actualmente desconocidos. Se limitan solamente a la investigación.
Titanio:
- Nombre: Titanio.
- Símbolo: Ti
- Número atómico: 22
- Masa atómica: 47,867 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 4
- Grupo: 4
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal de transición.
- Características más importantes del elemento: es el elemento metálico que posee la mayor proporción de dureza-densidad. Es un metal fuerte, con una baja densidad y alta ductilidad (especialmente en ambientes libres de oxígeno), de color blanco metálico. Su punto de fusión es relativamente alto, sobre los 1650 °C (1920 K), lo que hace que sea útil como metal refractario. Es paramagnético y presenta baja conductividad eléctrica y térmica.
- Aplicaciones: el titanio se emplea en las aleaciones de acero para reducir la cristalinidad y como desoxidante, y en las de acero inoxidable para reducir su contenido de carbono. Son frecuentes también las aleaciones con aluminio, vanadio, cobre, hierro, manganeso, molibdeno y otros metales.
Cromo:
- Nombre: Cromo.
- Símbolo: Cr
- Número atómico: 24
- Masa atómica: 52,00 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 4
- Grupo: 6
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal de transición.
- Características más importantes del elemento: el cromo es un metal de transición duro, frágil, color blanco agrisado y brillante. Es muy resistente frente a la corrosión.
- Aplicaciones: el cromo se utiliza principalmente en metalurgia para aportar resistencia a la corrosión y un acabado brillante. En aleaciones, por ejemplo, el acero inoxidable es aquel que contiene más del 12 % de cromo, aunque las propiedades antioxidantes del cromo empiezan a notarse a partir del 5 % de concentración. Además tiene un efecto alfágeno, es decir, abre el campo de la ferrita y lo fija. En procesos de cromado (depositar una capa protectora mediante electrodeposición). También se utiliza en el anodizado del aluminio.
Hierro:
- Nombre: Hierro.
- Símbolo: Fe
- Número atómico: 26
- Masa atómica: 55,845 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 4
- Grupo: 8
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal de transición.
- Características más importantes del elemento: es un metal maleable, de color gris plateado y presenta propiedades magnéticas; es ferromagnético a temperatura ambiente y presión atmosférica. Es extremadamente duro y denso. Se encuentra en la naturaleza formando parte de numerosos minerales, entre ellos muchos óxidos, y raramente se encuentra libre. Para obtener hierro en estado elemental, los óxidos se reducen con carbono y luego es sometido a un proceso de refinado para eliminar las impurezas presentes.
- Aplicaciones: el hierro puro (pureza a partir de 99,5 %) no tiene demasiadas aplicaciones, salvo excepciones para utilizar su potencial magnético. El hierro tiene su gran aplicación para formar los productos siderúrgicos, utilizando éste como elemento matriz para alojar otros elementos aleantes tanto metálicos como no metálicos, que confieren distintas propiedades al material. Se considera que una aleación de hierro es acero si contiene menos de un 2,1 % de carbono; si el porcentaje es mayor, recibe el nombre de fundición. El acero es indispensable debido a su bajo precio y tenacidad, especialmente en automóviles, barcos y componentes estructurales de edificios. Las aleaciones férreas presentan una gran variedad de propiedades mecánicas dependiendo de su composición o el tratamiento que se haya llevado a cabo.
Níquel:
- Nombre: Níquel.
- Símbolo: Ni
- Número atómico: 28
- Masa atómica: 58,69 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 4
- Grupo: 10
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal de transición.
- Características más importantes del elemento: es un metal de transición de color blanco con un ligerísimo tono amarillo, conductor de la electricidad y del calor, muy dúctil y maleable por lo que se puede laminar, pulir y forjar fácilmente, y presentando ferromagnetismo a temperatura ambiental. Es otro de los metales muy densos como el hierro, iridio y osmio. Se encuentra en distintos minerales, en meteoritos (aleado con hierro) y, en principio, hay níquel en el interior de la Tierra principalmente en su núcleo, donde se trata del segundo metal más abundante por detrás del hierro, metal con el que comparte numerosas características similares.
- Aplicaciones: aproximadamente el 65 % del níquel consumido se emplea en la fabricación de acero inoxidable austenítico y otro 12 % en superaleaciones de níquel. El restante 23 % se reparte entre otras aleaciones, baterías recargables, catálisis, acuñación de moneda, recubrimientos metálicos y fundición.
Cobre:
- Nombre: Cobre.
- Símbolo: Cu
- Número atómico: 29
- Masa atómica: 63,55 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 4
- Grupo: 11
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal de transición.
- Características más importantes del elemento: el cobre cuyo símbolo es Cu, es el elemento químico de número atómico 29. Se trata de un metal de transición de color cobrizo (rojizo) y brillo metálico que, junto con la plata y el oro, forma parte de la llamada familia del cobre, se caracteriza por ser uno de los mejores conductores de electricidad (el segundo después de la plata).
- Aplicaciones: el cobre se utiliza tanto con un gran nivel de pureza, cercano al 100 %, como aleado con otros elementos. El cobre puro se emplea principalmente en la fabricación de cables eléctricos.
Plata:
- Nombre: Plata.
- Símbolo: Ag
- Número atómico: 47
- Masa atómica: 107,87 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 45
- Grupo: 11
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal de transición.
- Características más importantes del elemento: es un metal muy dúctil y maleable, algo más duro que el oro, y presenta un brillo blanco metálico susceptible al pulimento. Se mantiene en agua y aire, si bien su superficie se empaña en presencia de ozono, sulfuro de hidrógeno o aire con azufre. Es el mejor conductor.
- Aplicaciones: el 70% de la producción mundial de plata se utiliza con fines industriales, y el 30%, con fines monetarios; buena parte de este metal se emplea en orfebrería, pero sus usos más importantes se dan en la industria fotográfica, química, médica, y electrónica.
Oro:
- Nombre: Oro
- Símbolo: Au
- Número atómico: 79
- Masa atómica: 196,97 u
- Si es sólido, líquido, gas a temperatura ambiente: es sólido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 6
- Grupo: 11
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal de transición.
- Características más importantes del elemento: el oro exhibe un color amarillo en bruto. Es considerado como el metal más maleable y dúctil que se conoce. Una onza (31,10 g) de oro puede moldearse en una lámina que cubra 28 m².Como es un metal blando, son frecuentes las aleaciones con otros metales con el fin de proporcionarle dureza.
- Aplicaciones: el oro puro o de 24k es demasiado blando para ser usado normalmente y se endurece aleándolo con plata y/o cobre, con lo cual podrá tener distintos tonos de color o matices. El oro y sus muchas aleaciones se emplean bastante en joyería, en relación con el intercambio monetario (para la fabricación de monedas y como patrón monetario), como mercancía, en medicina, en alimentos y bebidas, en la industria, en electrónica y en química comercial.
Mercurio:
- Nombre: Mercurio.
- Símbolo: Hg
- Número atómico: 80
- Masa atómica: 200,59 u
- Si es sólido, líquido, gas a temperatura ambiente: es líquido a temperatura ambiente.
- Si es natural o sintético: es natural.
- Periodo: 6
- Grupo: 12
- Metal ligero, metal de transición, metal, no metal o gas noble: es un metal de transición.
- Características más importantes del elemento: es un metal pesado plateado que a temperatura ambiente es un líquido inodoro. No es buen conductor del calor comparado con otros metales, aunque es buen conductor de la electricidad. Se alea fácilmente con muchos otros metales como el oro o la plata produciendo amalgamas, pero no con el hierro. Es insoluble en agua y soluble en ácido nítrico. Cuando aumenta su temperatura -por encima de los 40 °C-, produce vapores tóxicos y corrosivos, más pesados que el aire por lo que se evapora creando miles de partículas en el vapor que al enfriarse se depositan de nuevo. Es dañino por inhalación, ingestión y contacto.
- Aplicaciones: el mercurio se encuentra en diversos productos de uso cotidiano, tales como termómetros, barómetros, lámparas fluorescentes y otros dispositivos.
No hay comentarios:
Publicar un comentario